Yaitu CO 3 2-adalah anion molekuler. Karena berbagi elektron mereka menunjukkan sifat fisik karakteristik yang meliputi.
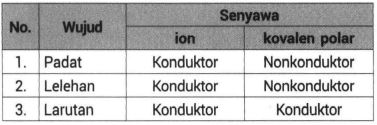
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po
Mereka juga memiliki sifatnya sendiri sehingga bisa menjadi pembeda dengan senyawa yang lain.

. Berikut adalah perbedaan antara ikatan kovalen dan ikatan Ion. Mudah larut dalam pelarut polar. Kalium Karbonat K2CO3 Ikatan Ion dan Kovalen K2CO3 2.
Senyawa ion yang terbentuk dari interaksi elektrostatik yang kuat antara ion yang menghasilkan titik leleh yang lebih tinggi dan konduktivitas listrik dibandingkan dengan senyawa kovalen. Senyawa kovalen berwujud lunak dan tidak mudah rapuh. Magnesium Hidroksida MgOH2 Ikatan Ion dan Kovalen MgOH2 4.
Di sisi lain senyawa kovalen non-logam yang terikat bersama-sama dan terdiri dari dua elektron yang dibagi antara dua atom. Negara-negara lain punya sistem penamaan trivial yang berbeda. Sebenarnya itu adalah jenis ikatan kimia terkuat yang ada.
Meski demikian senyawa kovalen dan ionik memiliki beberapa perbedaan dalam menghantarkan arus listrik. Contohnya asam klorida HCl Amonia NH35. Natrium Bikarbonat NaHCO3 Ikatan Ion dan Kovalen NaHCO3 6.
Rumus Derajat Ionisasi Contoh Soal Materi Kimia Kelas 10. Senyawa ionik cenderung padat di alam dan mereka biasanya memiliki titik leleh yang sangat tinggi karena ikatan ioniknya cukup kuat. Contoh senyawa ion adalah NaCl KCl NaOH dan KOH5 Senyawa kovalen polar.
Baik atom logam maupun atom non-logam terlibat dalam pembentukan ikatan ion sementara pada pembentukan ikatan kovalen. I2 dan gula bCair contoh. Senyawa Ionik dan Kovalen.
Senyawa kovalen polar apabila dilarutkan dalam air maka akan terurai menjadi ion-ion. Hal tersebut disebabkan oleh ikatan kovalen pada senyawa tersebut mudah putus dalam pelarut air dan menghasilkan ion-ion. PERBANDINGAN SENYAWA KOVALEN DAN SENYAWA IONIK Ikatan ion merupakan ikatan antara ion positif dan ion negatif yang terjadi karena partikel yang muatannya saling berlawanan akan mengakibatkan terjadinya tarik menarik antar ionion tersebut.
Perilaku ini dipengaruhi oleh jenis ikatan yang terjadi pada senyawa NaCl garam dapur yaitu. Garam dapur NaCl merupakan pola paling sederhana dari suatu senyawa ionik. Hanya atom non-logam yang.
Pada umumnya ikatan ion terbentuk antara atom logam yang mudah melepaskan elektron ion. Natrium Hipoklorit NaClO Ikatan Ion dan Kovalen NaClO 3. Senyawa ionik adalah senyawa yang atom-atomnya berikatan secara ionik.
Perbedaan Antara Ikatan Ion Kovalen dan Logam Definisi. Definisi dasar dari suatu senyawa ionik adalah bahwa mereka adalah molekul yang terdiri dari ion bermuatan. Dua jenis ikatan adalah ikatan ion dan ikatan kovalen.
Apa yang membedakan Ikatan ion dan kovalen. Namun sistem trivial menyebutnya garam dapur atau halit. Karena itu menurut definisi ikatan ion terbentuk antara anion dan kation.
Ikatan kovalen relatif lunak dan rapuh dibandingkan dengan ikatan ion yang keras. Ion positif dan ion negatif akan terbentuk apabila terjadi serah terima elektron antar atom. Sifat senyawa ion maupun sifat senyawa kovalen dapat kita jabarkan sebagai berikut.
Dalam ikatan kovalen atom terikat oleh elektron yang dibagi. Ikatan ionik adalah ikatan yang dihasilkan dari perpindahan elektron dari satu atom ke atom lain. Perbedaan antara mereka ada hubungannya dengan seberapa sama atom yang berpartisipasi dalam ikatan berbagi elektron mereka.
Dalam ikatan kovalen orbital elektron tumpang tindih sementara ini terpisah dalam kasus ikatan ion. Secara umum perbedaan senyawa ionik dan kovalen dijelaskan oleh tabel di bawah ini. Lelehan wujud ini dapat menghantarkan listrik karena dalam bentuk lelehan ion-ionnya bergerak relatif bebas.
Ikatan ion adalah gaya elektrostatik yang timbul antara ion negatif dan positif. Perbedaan antara senyawa ionik dan kovalen dapat membingungkan. Berikut ini akan dibahas mengenai perbedaan sifat fisika senyawa ion dan senyawa kovalen yang meliputi titik leleh dan titik didih kemudahan menguap volatile daya hantar listrik dan kelarutan.
Berikut ini adalah penjelasan mengenai ikatan ion dan ikatan kovalen. Suatu molekul atau senyawa dibuat ketika dua atau lebih atom membentuk ikatan kimia yang menghubungkannya bersama. Senyawa kovalen tidak larut dalam pelarut polar namun larut dalam pelarut organik.
Begitu juga dengan senyawa ion dan kovalen. Ion-ion ini memiliki muatan berlawanan negatif dan positif. Kalium Sulfat K2SO4 Ikatan Ion dan.
Ikatan logam adalah gaya antara elektron. Ikatan ion elektrovalen adalah ikatan yang terjadi antara ion positif dan ion negatif dalam suatu senyawa dan terjadi serah terima elektron dari satu atom ke atom lain. Anda dapat memprediksi ikatan ionik akan terbentuk ketika dua atom memiliki nilai keelektronegatifan yang berbeda dan mendeteksi senyawa ionik berdasarkan sifat-sifatnya termasuk kecenderungan untuk berdisosiasi menjadi ion-ion dalam air.
Kovalen Non Polar larut dengan pelarut non polar contoh. HF asam florida. HCl H2SO4 Br2 cGas contoh.
Titik didih dan titik leleh tinggi. Trik Super Kilat Membedakan Senyawa Ion dan Senyawa KovalenCara cepat dan muda membedakan senyawa ion dan senyawa kovalenOk sahabat Dg Tiro atau adik-ad. Ikatan kovalen adalah ikatan yang terjadi ketika dua elemen berbagi elektron valensi untuk mendapatkan konfigurasi elektron gas netral.
Senyawa kovalen tidak dapat menghantarkan listrik. Sistem penamaan ini hanya berlaku di Indonesia saja. Untuk memahami perbedaan wujud senyawa ionik dan kovalen polar ini berikut penjelasannya.
Natrium Hidroksida NaOH Ikatan Ion dan Kovalen NaOH 5. Senyawa kovalen memiliki titik didih dan titik leleh yang rendah. Satu atom memberikan satu atau lebih dari elektron.
Hal ini disebabkan oleh cara pembentukan ikatan yang berbeda. Sifat fisis senyawa ion umumnya berbeda dengan senyawa kovalen. Padatan wujud ini tidak dapat menghantarkan listrik karena dalam bentuk padatan tidak ada ion yang bergerak secara bebas.
Contohnya pada sistem IUPAC senyawa NaCl dinamakan natrium klorida. CO2 O2 H2 Cl2 2Kelarutan Mudah larut dalam pelarut polar maupun pelarut non polar. Senyawa kovalen memiliki ikatan di mana elektron dibagi antara atom.
Dalam ikatan kovalen sejati nilai-nilai. Pada Ikatan Kovalen 1Bentuk Senyawa yang dapat terjadi. Ion dapat berupa atom atau molekul.
Maka NaCl mempunyai semua sikap sebagai senyawa ionik.

Sebutkan 5 Contoh Perbedaan Antara Senyawa Ion Dan Senyawa Kovalen Brainly Co Id

Perbedaan Senyawa Ion Senyawa Kovalen Dan Lo Utakatikotak Com

Pengertian Senyawa Kovalen Polar Dan Nonpolar Serta Perbedaannya

Sebutkan Sifat Atau Ciri Senyawa Kovalen Dan Ion Brainly Co Id

Ikatan Ion Pengertian Proses Pembentukan Keunikan Contoh

Pengertian Sifat Dan Contoh Dari Senyawa Ion Panduan Kimia Riset

Buat Yang Kelas 10 Yuk Mengenal Ikatan Ikatan Kimia Dalam Atom
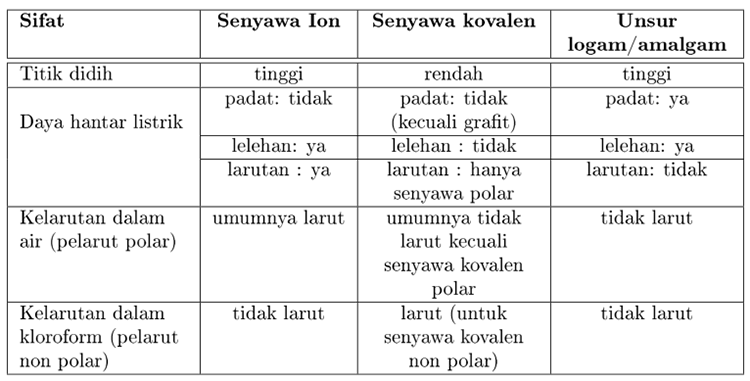
Modul Rumus Soal Sifat Fisis Senyawa Wardaya College
![]()
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po

Perbedaan Senyawa Ionik Dan Kovalen Penjelasan Materi Lengkap Hisham Id
.jpg)
3 Jenis Ikatan Kimia Ikatan Ion Ikatan Koval Utakatikotak Com

Pengertian Senyawa Kovalen Contoh Sifat Dan Rumus Senyawa

Ciri Ciri Dari Senyawa Ion Dan Senyawa Kovalen Brainly Co Id

Bandingkan Sifat Senyawa Ionik Dan Senyawa Kovalen
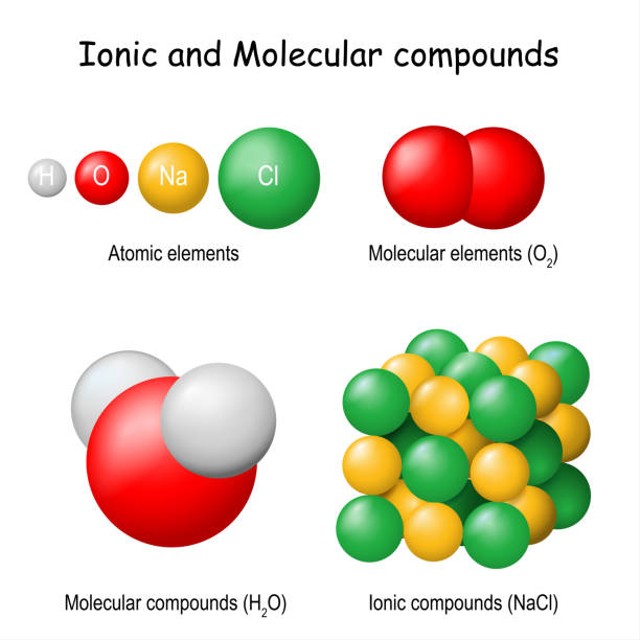
Perbedaan Senyawa Ionik Dan Senyawa Kovalen Polar Kumparan Com

Perbedaan Senyawa Ion Dan Senyawa Kovalen Youtube

Trik Super Kilat Membedakan Senyawa Ion Dan Senyawa Kovalen Youtube

C Tatanama Senyawa Kovalen Endah21zuraidah

Top 10 Jelaskan Perbedaan Daya Hantar Listrik Dari Senyawa Ion Dan Senyawa Kovalen Yang Berupa Padatan 2022
